本文是医学论文,具体研究结果总结如下:1.同时,纳米银抑制端粒复合体中TRF1、TRF2、POT1蛋白表达,使端粒复合体不能正确组装到端粒上,导致端粒功能紊乱。通过调控端粒酶与端粒的结构与功能可以调节肿瘤细胞对纳米银的敏感性;干扰或者抑制端粒酶催化亚基的表达,破坏端粒复合体的正确组装,使端粒结构异常,端粒酶不能正常结合到端粒上,都可使肿瘤细胞对纳米银的细胞毒性更敏感。纳米银长期暴露发现,虽然细胞增殖受到抑制,但肿瘤细胞中端粒酶活性上升,端粒出现小幅度的延长;端粒延长与端粒酶活性上升可能会提高肿瘤细胞对纳米银的抗性。对于纳米银应用导致的生物安全性问题,低剂量长期效应研究尚少,但其重要性不可忽视,本研究以细胞衰老作为生物学终点研究了纳米银低剂量长期暴露的肺组织毒性,证实了细胞衰老作为长期低剂量效应的终点是合适的;通过慢病毒转染系统及反转录病毒转染系统构建端粒/端粒酶功能和结构异常的细胞,揭示调控端粒/端粒酶对于肿瘤细胞响应纳米银细胞毒性的影响
....
第1章绪论
同时,纳米银在医学领域的应用,也对其生物效应及生物相容性提出了更高的要求,迫切需要对纳米银在细胞、组织和器官中的潜在毒性进行评估。人体接触纳米银的主要途径包括皮肤接触、吸入、摄入和注射。吸入是纳米银在生产制造或使用过程中进入人体的主要途径之一,纳米颗粒进入肺部后可能会与上皮细胞和肺巨噬细胞发生相互作用,从而导致肺部疾病;在肺部沉积的纳米银可能诱导细胞坏死、凋亡或基因突变,对这些组织或器官产生潜在毒性,进而引发肺炎和哮喘。虽然有很多研究关注吸入纳米银对肺组织的毒性效应,但是急性高剂量的暴露模式与实际暴露情况相距甚远,得到的结果也不能反映真实环境中纳米银对肺部的毒性效应;纳米银进入肺组织后会通过扩散或者巨噬细胞内吞等方式被细胞摄入,导致纳米银在组织中沉积,有研究显示,纳米银暴露56天后,仍在肺巨噬细胞中观察到纳米银存在;因此,必须充分评估低剂量纳米银的长期效应。

....
第2章材料与方法
2.1实验材料
端粒酶是一种核糖核蛋白复合物,其典型作用是维持端粒长度,在大多数癌症类型中被重新激活,它对癌细胞的持续增殖有很重要的作用。端粒长度随着细胞分裂而逐渐缩短,低于阈值后导致染色体不稳定、复制性衰老或凋亡。为了实现细胞的永生化,癌细胞中的端粒酶被重新激活,维持着端粒的稳定性。实验发现,缺乏端粒酶的小鼠对癌症有抵抗力,而在不同小鼠模型中端粒酶异位过表达与自发性肿瘤有关这些发现表明端粒酶和端粒在癌变过程中发挥关键的作用,这为抗癌治疗开辟了新的途径。大量研究显示,抑制端粒酶活性可能会限制肿瘤细胞的生长,提示端粒和端粒酶是癌症治疗的潜在治疗靶点。在此背景下,一些抗端粒酶和端粒的小分子被开发成高效的抗肿瘤分子.目前,己有许多研究报道了纳米银的抗肿瘤活性及分子机制,但很少能提供可调控的靶点,仅局限于纳米银的细胞毒性作用;本研究虽然发现可以通过端粒/端粒酶调控肿瘤细胞对纳米银细胞毒性的敏感性,但是仍存在不足,需要更深入的研究。然而,对于其他器官是否合适,以及研究中的一些待解决问题仍需进一步的探索。
2.2主要试剂、抗体、耗材和仪器
己有研究报道,纳米银低剂量长期暴露导致的毒性效应主要是炎症反应,与MAPK信号传导和促炎细胞因子产生有关;然而,炎症反应可能导致的病理变化并没有得到体内结果的验证;另外,炎症的特性是产生快,消退也快,并不能反映纳米银导致的病理变化。因此,亟需寻找更合适的生物学终点和病理终点来研究纳米银的肺组织毒性。利用转录组测序探索纳米银介导细胞衰老的关键信号通路;通过检测相关蛋白表达及合成产物验证转录组数据的分析结果;探索调控纳米银介导细胞衰老的信号通路是否能减轻或者预防纳米银诱导细胞衰老的作用;以小鼠为研究模型,通过检测肺组织中蛋白表达及胶原沉积,探究纳米银吸入暴露是否会导致肺组织发生衰老相关的慢性疾病。应用COX2抑制剂可以消除纳米银的细胞衰老诱导效应,相应的COX2表达及PGE2含量都与耒处理组无差异;NFkB/COX2/PGE2信号通路参与纳米银诱导的细胞衰老过程,通过COX2可调控纳米银的细胞衰老效应

第3章纳米银调控端粒/端粒酶发挥抗肿瘤活性.....................37
3.1引言.....................37
3.2实验结果.....................38
第4章低剂量纳米银长期暴露对肺细胞衰老的影响及机制研究.....................57
4.1引言.........................57
4.2实验结果.....................58
4.3讨论.....................81
第5章总结与展望.....................86
.....
第4章低剂置纳米银长期暴露对肺细胞衰老的影响及机制研究
4.1引言
细胞衰老是指细胞在受到各种不同的刺激时发生永久的生长停滞的一种特殊现象[264]。衰老细胞会激活复杂的旁分泌反应,包括细胞因子、趋化因子、生长因子、蛋白酶和细胞外基质重塑因子[265]。这些衰老相关分泌表型(SASP)中的细胞因子通过反馈机制影响细胞微环境,加速衰老过程[266]。最初,认为是过度的细胞增殖(复制性衰老)、错误的的原癌基因激活(过早衰老)和DNA损伤反应(DDR)导致了细胞衰老值得注意的是,衰老的肺细胞参与了特发性肺纤维化(IPF)的病因或疾病发展[268]。越来越多的证据表明,暴露于各种有毒物质(如香烟烟雾和金属纳米颗粒)可显著加速细胞衰老并诱发衰老相关的慢性疾病。WORThINGTON等人证明,暴露于纳米铜颗粒会诱发肺组织急性炎症反应,并导致IPF[269]。在另7项研究中,观察到暴露于纳米银后肺部出现中度炎症反应和衰老这些发现表明细胞衰老是纳米材料使用过程中的潜在生物学效应。
4.2实验结果
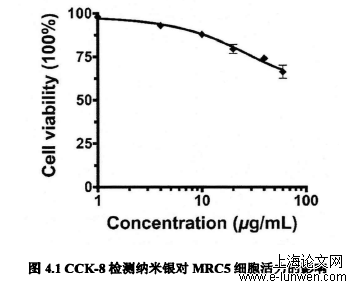
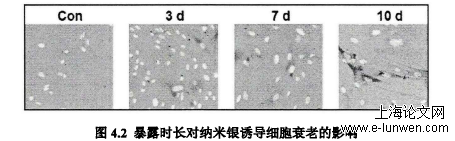
本章节中,基于纳米银呼吸系统暴露及细胞衰老在肺损伤和慢性疾病发展中的重要性,以人胚肺成纤维细胞(MRC5)及C57BL/6位研究对象,利用蛋白免疫印迹、细胞免疫荧光、ELISA、免疫组织化学并结合细胞衰老检测方法,本研究以细胞衰老为终点研究纳米银长期、低剂量暴露的潜在肺毒性及机制。这项研究将为纳米银对人类呼吸系统的毒理学作用提供新的见解。本章以人胚肺成纤维细胞及C57BL/6小鼠为研究模型,探究纳米银诱导正常细胞及小鼠肺组织细胞衰老效应及机制。揭示了纳米银导致肺炎症反应与病理变化之间的关系,找到了纳米银细胞衰老效应的调控靶点,为评估纳米银低剂量长期暴露的肺毒性效应提供新的研究思路,具体结果如下(图4.30):1.亚毒性浓度纳米银暴露导致时间依赖性细胞增殖抑制,短期没有显著的抑制效应;纳米银长期暴露诱导SASP因子表达上调,染色质出现异常凝集(SAhF),灸半乳糖苷酶活性上调等衰老相关的标志,且观察到细胞体积变大、核体积增大等形态学变化;纳米银暴露导致显著的细胞衰老;2.纳米银暴露后COX2/P65表达上调,培养液中PGE2含量显著增多,与细胞衰老趋势一致;3.长期暴露于纳米银导致细胞周期停滞于G2/M期,但这种变化在应用COX2抑制剂后并未消除;COX2作用于细胞周期之后的过程
.........
第5章总结与展望
2.低剂量纳米银长期暴露对肺衰老的影响及机制纳米银对正常肺细胞毒性:对于低剂量纳米银暴露而言,短期没没有显著的细胞毒性,随时间延长,细胞增殖受到抑制、DNA损伤、染色质异常凝集,表现出衰老表型,随后衰老细胞通过凋亡途径被清除;纳米银暴露激活NF/CB信号通路,P65结合到C0X2启动子上调C0X2表达,进而合成更多的PGE2介导炎症反应并激活衰老信号,导致细胞发生衰老。通过C0X2抑制剂可以调控正常细胞对纳米银衰老效应的应答,减轻纳米银对正常细胞的毒性效应。纳米银吸入肺组织后在肺组织中沉积,电镜观察到纳米银主要富集在细胞的脂滴结构中;吸入.纳米银导致肺组织出现炎症、胶原沉积、衰老细胞增多等表现,炎症反应与衰老细胞增多可能与胶原沉积及肺纤维化有关。研究机制上,从端粒/端粒酶调控肿瘤细胞存活出发,研究纳米银发挥肿瘤细胞毒性效应的机制,通过调控端粒/端粒酶的活性及功能增强纳米银对肿瘤细胞的毒性;从细胞命运角度出发,通过应用抑制剂,揭示了C0X2调控位点在细胞周期下游,细胞衰老及凋亡的上游;技术方法上,通过转录组分析迅速锁定低剂量纳米银长期暴露诱导衰老的关键因子,应用衰老-凋亡共染方法揭示纳米银诱导的衰老细胞通过凋亡途径被清除。
参考文献(略)
参考文献(略)

