本文是一篇毕业论文,毕业论文,泛指专科毕业论文、本科毕业论文(学士学位毕业论文)、硕士研究生毕业论文(硕士学位论文)、博士研究生毕业论文(博士学位论文)等。(以上内容来自百度百科)今天为大家推荐一篇毕业论文,供大家参考。
前 言
随着现代技术的迅猛发展,人们从自然界繁多的物种中获得了无数宝贵的具有重要生物活性的天然产物,生物碱便是重要的代表之一。它们大多存在于植物中,具有复杂的氮杂环结构,通常呈弱碱性并具有光学活性。现今已知的生物碱约有 10,000 种左右,人们依据基本结构骨架将其分为有机胺、喹唑酮、异喹啉、莨菪烷及甾体与萜等十二类[1]。生物碱大多具有重要的药理活性,其中异喹啉类生物碱已被发现具有消炎抗菌、抗癌、调节免疫及保护心脑血管等诸多功效,在临床治疗中发挥了重要作用[2]。比如:莲心碱的季铵盐形式有缓慢持久的降压作用;粉防己碱可对抗有机磷中毒;小檗碱对Ⅱ型糖尿病有较好的疗效。异喹啉类生物碱有相当一部分来源于罂粟种属植物,其乳汁及果壳中均含有大量生物碱,代表性的有罂粟碱、吗啡及可待因。有研究表明罂粟碱能够抑制 HIV 复制,对艾滋病有很好疗效[2];而吗啡及其衍生物是临床上非常重要的镇痛剂;可待因则有镇咳、催眠及兴奋中枢神经系统的作用[3]。这些重要的药理作用及临床应用引起了国内外学者对罂粟种属植物中提取的异喹啉类生物碱的关注,相关的分离分析、生物活性及化学合成研究成果层出不穷。
本文研究的异杷碱类生物碱便是来源于罂粟种属植物的异喹啉类生物碱,它们具有以异喹啉为核心的双苯并氮杂二环[3.2.2]壬烷结构(图 1)。中药药理活性测定其有止痛、镇咳、镇静的作用,已有研究显示其对于治疗 Alzheimer 症,Parkinson症,唐氏综合症及 Huntinton 舞蹈症等神经系统紊乱性疾病有较好疗效[4]。然而,天然异杷碱获取困难,仅仅依靠从罂粟种属植物中提取成本太高,操作复杂且过程漫长,极大地限制了对其生物活性的进一步研究。于是研究人员把目光转向了异杷碱类生物碱的化学合成,但自五十年代被发现至今异杷碱类生物碱的化学合成研究进展缓慢,与其他生物碱层出不穷的多种多样简便高效的合成方法相比,天然异杷碱类生物碱的化学合成方法报道较少,且多借助于手性诱导或手性源合成,往往存在成本高、步骤长、难于大量生产等缺点,实用性较差。不对称催化反应作为合成光学活性化合物主要方法之一,与其它方法相比较具有手性增值、简便、高效等优点。目前仅有 1 篇关于用不对称催化反应合成异杷碱类生物碱的报道,但该方法需要近二十步反应,总产率仅 3.3%[5]。本文成功探索出一条利用绿色高效的不对称催化技术合成光学纯异杷碱类生物碱的新方法,以芳香醛为起始原料经十步反应获得最终产物。经实验验证该方法可有效用于合成一系列天然及非天然异杷碱类生物碱,为满足科研及医疗需求开辟了一条新途径。
..........
文献回顾
1 天然异杷碱类生物碱的分离及结构确认
现今,人们从罂粟种属植物中获取的天然异杷碱种类并不多,其结构见图 2,它们从最初被发现到最终的结构确认经历了近十年时间,凝聚了诸多科研工作者的辛勤付出,这个过程既包含了失望又充满着惊喜。1960 年,Boit 和 Flentje 从罂粟种属植物裸茎中首次提取出一种具有苯酚结构的化合物,并将其命名为 Amurensine,因所得数据有限,他们仅根据研究经验推测出了该化合物的分子式,未能确定其结构[6]。两年后 Santavf 小组从罂粟种属植物中又分离出一类似化合物,命名为 Xanthopetaline。但两年后该小组最终确认了Xanthopetaline 与 Boit 前期报道的 Amurensine 为同一化合物,并将其定名为Amurensine[7]。同时他们开展了 Amurensine 的结构确认工作,Amurensine 经过甲基化作用可以转变为非酚类化合物 Amurensinine(其结构见图 2),光谱数据及降解分析结果与通过化学方法合成出的异杷碱完全一致,这意味着异杷碱类生物碱在罂粟种属植物中首次被发现[8, 9]。1966 年 Hruban 通过化学及生物合成等方法判定了Amurensine 中酚羟基的位置,并通过大量光谱分析[10]及全合成方法加以确认[11]。Yunusov 和 Akramov 于 1966 年从红花疆罂粟中分离出来第一个季铵盐形式的异杷碱(-)-Remrefine,其结构见图 2。在发现之初,(-)-Remrefine 曾被误认为具有杷碱的结构骨架。之后两年间,Yunusov 和 Akramov 依据次级霍夫曼降解产物及相关的 质 谱 分 析 对 (-)-Remrefine 的 结 构 进 行 了 修 正[12]。 随 着 (-)-Reframidine 、(-)-Reframine 、(-)-Reframoline 三种新型异杷碱的发现(见图 2),加之将人工合成物与植物提取的 Reframine 的季铵盐进行光谱对比,最终证明了(-)-Remrefine 是(-)-Reframine 的季铵盐类似物。1969年Kupchan和 Yoshitake 从唐松草属植物中提取出(-)-Thalisopavine(图2),并通过光谱分析和全合成对其结构进行了确认[13]。
..........
2 异杷碱类生物碱的药理作用
由于罂粟种属植物中天然异杷碱含量低且提取困难,关于其生物活性研究的报道十分有限。已有的中药药理活性测定显示其具有止痛、镇咳、镇静的作用,对于治疗 Alzheimer 症,Parkinsonismus 症,唐氏综合症及 Huntington 舞蹈症等神经系统紊乱性疾病有较好疗效[4]。仅仅依靠从罂粟种属植物中提取成本太高,操作复杂且过程漫长,极大地限制了对异杷碱类生物碱的进一步研究和开发,于是人们将目光转向了异杷碱类生物碱的化学合成,早在 1955 年,Guthrie 小组报道了一个合成吡咯啉杂环的新方法,使用硫酸处理取代的亚基乙缩醛衍生物 2 可得到吡咯啉杂环衍生物 3[14](图 3)。1958 年,Battersby和Yeowell等通过Hofmann降解产物的化学分析及紫外光谱等手段证明了Guthrie的报道是错误的。事实上,使用上述方法得到的并非吡咯啉衍生物 3,而是一个含有四氢异喹啉母核的双苯并氮杂二环[3.2.2]壬烷 4,他们将其命名为 Isopavine,即异杷碱[9],这是异杷碱结构及合成方法的首次报道。
............
第二章 不对称 MBH 反应新型底物初探.............69
1 背景介绍..................69
1.1 不对称 Morita-Baylis-Hillman 反应................69
1.2 不对称 MBH 反应的底物类型..........70
2 催化反应条件探索........... 72
2.1 催化剂的筛选............... 72
2.2 溶剂的筛选................73
2.3 温度与底物配比的筛选............73
2.4.小结.......76
3.实验部分..................77
3.1 实验通则.............77
3.2 实验方法.............77
第二章 不对称 MBH 反应新型底物初探
1 背景介绍
手性(Chirality)表示的是物质的不对称性,它普遍存在于宇宙,例如行星自转公转均为右旋,天然的糖均为 D-构型。生命现象也与手性紧密相关,人体内的氨基酸都是左旋体,由左旋氨基酸构成的蛋白质也便与手性密不可分。这就决定了药物活性成分在体内作用时其立体构型十分重要,因为代谢及吸收方式的不同,一对对映体在体内可能呈现出截然相反的作用,一种构型可以有效对抗疾病,而另一构型则可能无效甚至有毒害作用。因此,人们非常看重单旋体手性药物的研发,而催化不对称合成因其绿色、简便、经济高效成为了药物研发及有机合成领域的重点研究方向。催化不对称合成技术可分为三大类:生物酶催化、不对称金属催化和不对称有机催化[58]。而其中研究最活跃的领域之一便是不对称有机催化。手性 C-C 键的构筑是不对称合成领域长期探索的问题,而不对称 MBH 反应是手性 C-C 键构筑最常用的方法。如图 32 所示,手性叔胺或叔膦催化活化烯烃与亲电试剂(醛、酮、亚胺)偶联,生成烯烃α-位加成的手性产物[59]。不对称 MBH 反应具有原子经济性高、产物官能团多、易于衍生化等优点,被广泛用于有机合成及天然产物全合成。此外,MBH产物还具有抗肿瘤、抗菌、抗真菌、抗疟、杀虫等多种生物活性,因此,该反应在新药研发及药物合成中的应用前景和发展潜力也日益受到人们的重视[60]。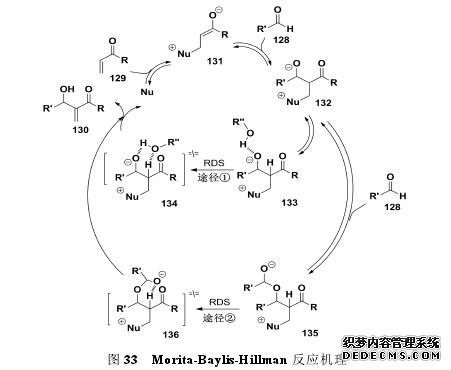

........
总结
本文主要包含了异杷碱类生物碱的不对称全合成新方法与不对称 MBH 反应新型底物初探两章内容。在第一章中,我们设计并成功探索出一条利用绿色高效的不对称催化技术合成光学纯异杷碱类生物碱的新方法。该方法以芳香醛为起始原料经十步反应获得最终产物,其中缩醛基芳香硝基烯与芳香硼酸的不对称加成反应为构建手性中心的关键步骤。现已成功合成出(-)-O-Methylthalisopavine、(-)-Amurensinine、(-)-Reframine、(-)-Reframidine、(-)-Thalidicine、(-)-Amurensine 六种天然异杷碱类生物碱及一种非天然异杷碱 120f。我们同时合成了上述七种异杷碱类生物碱的外消旋产物作为对照品,建立了异杷碱类生物碱光学纯度的手性 HPLC 测定方法,测定了上述七种异杷碱类生物碱的 ee 值分别为 95.3%、96.1%、95.9%、95.1%、96.9%、96.1%、96.5%。与已报道的光学纯异杷碱类生物碱不对称全合成方法相比,我们的全合成路线具有以下优势。①从初始原料到终产物共需十步反应,每步实验均为常规操作,且产率较高,适合大量合成;②合成原料价格低廉,仅用少量手性催化剂便可获得大量光学纯产物,实现了手性增值,更经济高效;③在合成中只需通过简单的取代基改变,即可制得不同结构的硝基烯及芳香硼酸底物。在同一催化剂作用下,仅将上述不同底物进行不同搭配,即可制备出不同种类的异杷碱类生物碱单旋体,整个合成路线具有高度积木化的特点。④在不对称催化反应一步选用不同构型的手性配体可制备不同构型的光学纯催化产物,进而通过相同的衍生化操作制备不同构型的光学纯异杷碱类生物碱,实用性强,适用范围广,产品光学纯度高。在上述研究结果的基础上,我们将继续利用该方法合成更多的天然及非天然异杷碱类生物碱,为异杷碱类生物碱的药学研究与开发奠定基础。第二章中我们首次实现了活性醛作为亲电试剂与共轭硝基烯的不对称 MBH 反应。考察了了基于金鸡纳生物碱骨架、二茂铁骨架、环己二胺骨架以及联萘骨架类等 21 种有机小分子手性催化剂对该反应的催化活性,发现金鸡纳生物碱骨架的小分子催化剂对乙醛酸乙酯与β-硝基烯的不对称MBH反应有较好催化效果。后通过温度、溶剂、底物比例等条件的筛选确定了最佳反应条件,在金鸡纳生物碱类催化剂(DHQ)2AQN 作用下,1 当量的β-硝基苯乙烯与 3 当量的乙醛酸乙酯 22 在甲苯中 0°C下反应,获得光学纯度为 56.9% ee 的 MBH 加成产物,化学产率 60%。#p#分页标题#e#
..........
参考文献(略)

